兽用中化药生产企业GMP监督检查情况分析与思考
|
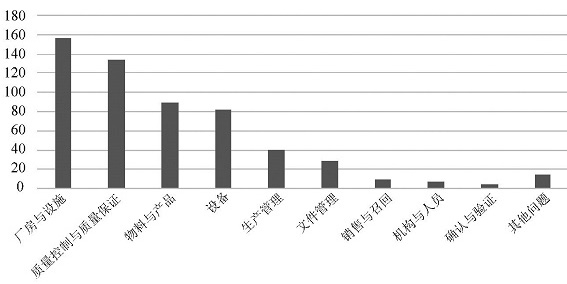
自2020年6月1日起,《兽药生产质量管理规范(2020年修订)(以下简称新版兽药GMP)正式实施,新版兽药GMP吸收借鉴国内外GMP先进经验,贯彻质量风险管理和兽药生产全过程管控的理念,要求建立完善的文件体系,在提升兽药生产企业管理能力,规范和促进兽药行业健康发展方面发挥了重要作用。为确保新版兽药GMP的有效实施,近年来兽药监管部门加大了对兽药生产企业的监管力度。本文对新版兽药GMP施行后中国兽医药品监察所(以下简称中监所)组织开展的中化药生产企业监督检查中发现的缺陷项目进行统计分析,为企业提升生产质量管理水平、完善质量管理体系提出一些建议,并供兽药监管部门参考。 一、检查实施情况 兽药生产企业GMP监督检查主要分为飞行检查和日常监督检查。2017年11月,农业农村部修订发布《兽药生产企业飞行检查管理办法》(农业部公告第2611号)。飞行检查是指兽医行政管理部门根据监管工作需要,对兽药生产企业实施的不预先告知的监督检查,具有突击性、针对性和高效性等特点,主要针对投诉举报、批准文号申报资料或样品涉嫌造假,以及可能存在重大质量安全风险等情况,属于有因检查。日常监督检查是指除飞行检查外的一些常规性检查,目前依据《中国兽医药品监察所兽药GMP日常监督检查工作程序》开展检查工作。像抗菌药专项检查、产品标签说明书专项检查、兽药生产许可事项实施情况专项检查等,均属于日常监督检查。农业农村部畜牧兽医局负责全国兽药检查工作的组织领导,中监所负责国家层面检查工作的具体实施。 自2020年起,中监所对兽用中化药生产企业开展了96次GMP监督检查,其中飞行检查23家次,派出检查人员71人次,发现缺陷139项;日常监督检查73次,派出检查人员222人次,发现缺陷429项。 兽用中化药生产企业GMP监督检查发现的缺陷项目分布情况 二、存在的主要问题 通过统计发现,缺陷项目主要集中在厂房与设施设备、质量控制与质量保证、物料与产品、生产管理等方面,缺陷项目分布情况见图所示。 1、厂房和设施方面 厂房和设施方面的缺陷项目占比最高(28%左右),主要表现在部分生产线厂房设施的设置不符合要求或日常维护管理不到位,如无菌制剂车间内缺少废弃物退出通道;粉剂/预混剂车间未设置中央除尘系统;移动料仓在混合间内进行清洗或清洗站面积过小;含氯消毒剂车间灯具、开关和排风设施不符合防爆要求;车间地面破损、房屋渗水、进入C级洁净区的互锁失效,未能及时维修。此外,部分企业洁净区环境监测的项目、频次或取样点位置不合理,且对多产品共线的评估不充分。一些兽用中药生产企业对于中药材前处理设置原则理解不到位,没有设置前处理车间(如拣选、干燥等工序)。 |
上一篇:兽药行业内卷下的危与机
下一篇:中小兽药企业如何突出重围?