新形势下中国猪场的非洲猪瘟防控
|
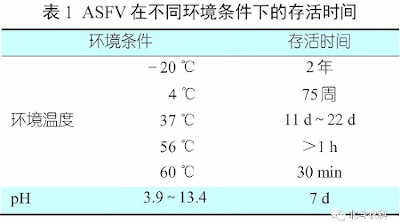
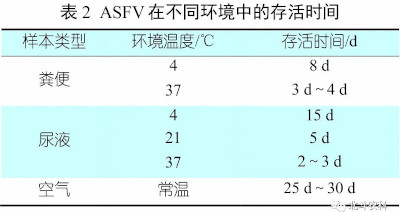
摘要:自2018年我国首次确诊非洲猪瘟疫情以来,各规模化猪场纷纷进行了非洲猪瘟防控的探索,根据非洲猪瘟病毒通过接触传播且传播速度慢的流行特点,有关猪场发明了精准清除策略,推广后得到了业内人员的广泛认可。然而随着非洲猪瘟病毒弱毒株和基因缺失株(又称为“疫苗株”)的出现,这一方法已经不如之前那样有效。本文通过对非洲猪瘟病毒的病原学、流行病学、实验室诊断以及精准清除策略的回顾,分析了当前猪场存在非洲猪瘟病毒强毒株、弱毒株和基因缺失株并存和干扰等现状,总结了非洲猪瘟诊断与防控策略。根据目前的情况,生物安全依然是预防非洲猪瘟最根本的方法,精准清除需要更加严格的采样和检测,对感染非洲猪瘟病毒弱毒株和疫苗株的猪群进行更专业的精准清除,同时需要加强对各种应激因素的控制,提高猪的抵抗力,减少非洲猪瘟病毒弱毒株潜伏感染猪的排毒量。希望本文能为我国防控和根除非洲猪瘟提供有益的参考。 关键词:非洲猪瘟;弱毒株;基因缺失株;精准清除;应激;综合防控 1 非洲猪瘟病毒介绍 1.1病毒和基因组 非洲猪瘟(African Swine Fever,ASF)是由非洲猪瘟病毒(African Swine Fever Virus,ASFV)感染猪后引起的一种急性、热性、高度传染性和高致死性烈性传染病,迄今为止尚无有效疫苗和药物可以预防与控制。目前已知的ASFV有8个血清群和24种基因型,我国主要流行的是基因Ⅱ型。ASFV的基因组大小约170 kb~190 kb,能够编码200多种蛋白质,其中包括50多种结构蛋白。电镜下ASFV粒子呈正二十面体,直径约为200 nm,主要由囊膜、衣壳、内膜、内核心壳和基因组五部分组成。 1.2 感染机理 ASFV主要通过直接接触途径侵入猪的呼吸道或消化道,病毒侵入猪体后在鼻咽部或扁桃体等部位进行增殖,随后大量增殖的病毒随着血液和淋巴感染全身组织和器官,引起组织器官出血、血栓、浆液性渗出,甚至急性坏死。有研究表明,单核-巨噬细胞表面的CD163分子与ASFV的感染相关,ASFV感染机体主要通过内吞作用实现,ASFV进入猪的机体后立即侵染机体的单核-巨噬细胞,在胞饮泡或内吞体内完成内体成熟过程,随之启动病毒的增殖。病毒粒子脱去病毒囊膜后,暴露的病毒内膜与体内膜融合,释放出病毒基因组,基因组在细胞质中完成复制、转录和翻译等一系列过程,最后,基因组和蛋白质组装完成后通过动力蛋白的运输作用,将组装完整的病毒粒子释放到细胞外,进行下一次感染。 1.3 理化特性 ASFV是囊膜病毒,不耐热、不耐强酸和强碱,可耐受的pH范围为3.9~11.5。在不同环境中,ASFV存活时间不同(表1)。ASFV在低温下稳定,对高温敏感,56 ℃ 70 min或60 ℃ 20 min可灭活。该病毒在血清中较稳定,在含25%血清温度为37 ℃的溶液中半衰期为24 h,在血清中耐酸碱性也增强,如在pH 13.4下仍可存活;在血液中,ASFV在低温条件下可存活6年,在室温下可存活数周。ASFV在猪的粪便和尿液中存活时间较短,在空气中的存活时间为25 d~30 d(表2),在猪肉制品中可长时间存活(表4),在猪的冷冻组织器官中可存活 6~12个月(表3)。 |
下一篇:吉林省无疫小区的建设与评估经验