当前非洲猪瘟疫苗的研发现状及创新策略
日期:09-29 作者:Teshale Teklue等,陈佳宁译- 小 + 大
|
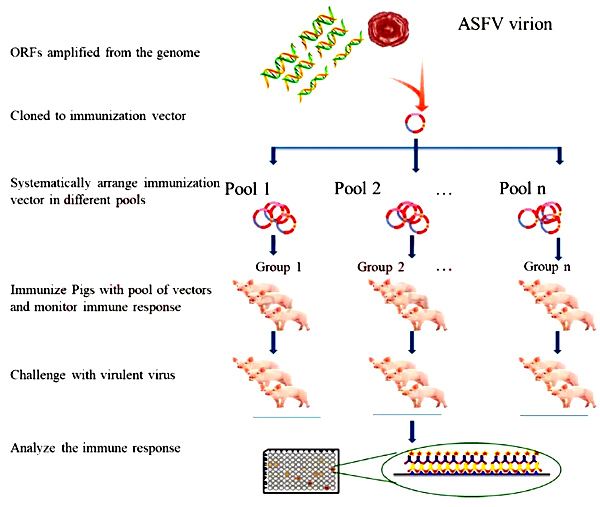
事实表明,多肽或DNA免疫无法提供全面的保护,一些研究团队提出了改进方法,例如DNA蛋白质疫苗接种策略。最近,ASFV质粒DNA(CD2v,p72,p32,+ /-p17)和重组蛋白(p15,p35,p54,+ /-p17)被联合用于猪的免疫;但是,未能保护猪免受ASFV的感染。Pérez-Núñez 等人报道了DNA蛋白质免疫有助于识别病毒抗原特异性反应,并提供了更安全的ASFV亚单位疫苗的潜在信息。 初免结合加强免疫是快速产生大量记忆性CD8 + T细胞的可行方法。因此,通过初免-加强接种,已筛选出多种具有免疫原性的ASFV抗原。用从人类胚胎肾293(HEK)细胞纯化的三种抗原B646L(p72)、E183L(p54)和O61R(p12)免疫猪,以及三个改造的经牛痘病毒Ankara载体携带的抗原B646L,EP153R和EP402R(CD2v)加强免疫,可诱导产生ASFV特异性抗体和T细胞应答。最近,DNA初次免疫和重组痘苗病毒增强免疫已用于筛选具有免疫原性和潜在保护性的ASFV抗原。在这个实验中,大约47个病毒基因被克隆到单个质粒中作为DNA疫苗,这些基因同时也被克隆到重组牛痘病毒中作为加强免疫疫苗。尽管接种后的猪在攻毒后出现了临床和病理症状,血液和一些淋巴组织的病毒载量与对照组相比显着降低。这种大规模、系统的抗原筛选将在研发新型ASFV亚单位疫苗中成为探索免疫原性和最佳免疫反应的路线图(图1总结)。 图1. ASF亚单位疫苗的开发方法:将病毒的靶基因通过PCR扩增并克隆到载体中进行免疫。然后,用ORF表达文库对猪群进行免疫。每个文库中克隆的抗原可以根据免疫反应的结果进一步分离评估。 目前,已鉴定出五十多种具有免疫原性的ASFV蛋白,其中包括最近报道的用于病毒包装的44种病毒多肽。尽管如此,这些新发现的蛋白的免疫原性仍然位未知。 开发ASF亚单位疫苗平台,相关的ASFV保护性抗原和现有病毒株多样性的需求仍有待探索。 通常,ASF亚单位疫苗诱导的保护并不完全,并且远远没有达到应用要求。但是,这些DNA疫苗或基于载体的疫苗平台具有多种优点,因为它们可以被安全地制造和使用,诱导广谱免疫反应,并且可被用作标记疫苗。 4.3天然和体外减毒疫苗 减毒活疫苗(LAV)是由病毒在非宿主动物体内或体外连续传代而成,已成功控制多种病毒性疾病。同样的,已经进行了各种尝试以天然或体外致弱的ASFV免疫猪。但是,在野外条件下,免疫了常规产生的ASF减毒活疫苗的猪只发生了出乎意料的并发症。而且,已经有研究表明适应Vero细胞的ASFV分离株可导致体内病毒复制减少以及病毒基因组基因缺失的逐渐积累。如今,分子生物学的显着进步已经使得人们可以更好地了解ASFV生物学的基本特征。因此,特定基因缺失的ASFV突变体为合理开发疫苗开辟了新的可能性(表2)。 |
上一篇:揭开“自家苗”的面纱!
下一篇:您关心的非瘟疫苗到底有没有?